जब दो भिन्न भिन्न हैलोजन भिलकर सहसंयोजी यौगिक बनाते हैं तो उसे
अंतराहैलोजन यौगिक कहते हैं |
कारण : हैलोजनों की ऋण विद्युतता में अंतर
सामान्य सूत्र : ABn
नामकरण :- सूत्र में जो हैलोजन बाद में लिखते हैं( B) उसके नाम में आइड लगाते हैं तथा पहले वाले( A) का सामान्य नाम इस्तेमाल करते हैं |एक से अधिक होने पर मोनो, डाई ,ट्राई ,पेंटा आदि प्रयोग करते हैं| Example- ClF का नाम क्लोरीन फ्लोराइड , ClF3 का नाम क्लोरीन ट्राई फ्लोराइड
अंतराहैलोजन यौगिकों के प्रकार :-
1- AB प्रकार के अंतराहैलोजन यौगिक
2- AB3 प्रकार के अंतराहैलोजन यौगिक
3- AB5 प्रकार के अंतराहैलोजन यौगिक
4- AB7 प्रकार के अंतराहैलोजन यौगिक
AB प्रकार के अंतराहैलोजन यौगिक
उदाहरण : ClF ,BrF, ICl etc
बनाने की अभिक्रिया : Cl2 + F2 ———> 2ClF (at 200oC)
ऑक्सीकरण अवस्था : +1
संकरण : sp3
संरचना या आकार : रेखीय
AB3 प्रकार के अंतराहैलोजन यौगिक
उदाहरण : ClF3
बनाने की अभिक्रिया : Cl2 + 3F2 ———> 2ClF3 (at 200oC)
ऑक्सीकरण अवस्था : +3
संकरण : sp3d
संरचना या आकार : T shape
AB5 प्रकार के अंतराहैलोजन यौगिक
उदाहरण : BrF5
बनाने की अभिक्रिया : Br2 + 5F2 ——-> 2BrF5 (at 50oC)
ऑक्सीकरण अवस्था : +5
संकरण : sp3d2
संरचना या आकार : वर्गाकार पिरामिडी
AB7 प्रकार के अंतराहैलोजन यौगिक
उदाहरण : IF7
बनाने की अभिक्रिया : 7IF5 —————->5IF7 + I2 ( long heating with Pt )
ऑक्सीकरण अवस्था : +7
संकरण : sp3d3
संरचना या आकार : पंचभुजी द्विपिरामिडी
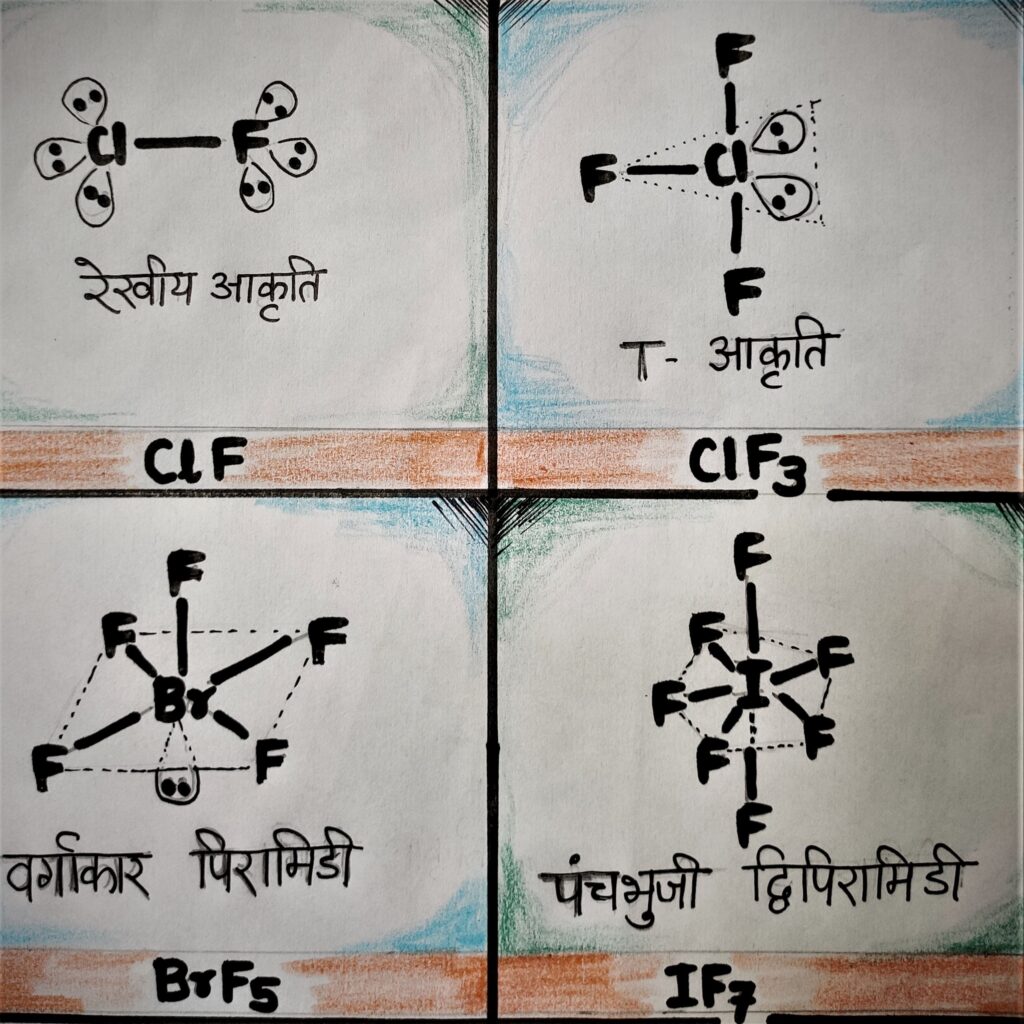
अंतराहैलोजन यौगिकों की संरचना , संकरण आदि को समझने के लिए ये वीडियो देखें
